Гидроксид меди(II) (Cu(OH)2) - это неорганическое соединение, в котором медь образует стехиометрический комплекс с гидроксидом. Оно обладает интересными свойствами и активно применяется в различных областях, от химической промышленности до медицины.
Одной из наиболее распространенных реакций гидроксида меди(II) является его растворение в воде. При этом образуется гидроксидный ион (OH-) и ион меди(II) (Cu2+). Это реакция обратима, что означает, что гидроксид меди(II) может осаждаться обратно из полученного раствора при изменении условий.
Кроме воды, гидроксид меди(II) реагирует с другими веществами, например, с кислотами. В результате таких реакций образуются соли меди(II). Например, реакция между гидроксидом меди(II) и соляной кислотой (HCl) приводит к образованию хлорида меди(II) (CuCl2).
Интересно, что гидроксид меди(II) также может быть использован в качестве катализатора для ряда органических реакций. Например, он может участвовать в окислительно-восстановительных реакциях, а также в гетерогенной делокализованной катализе. Это делает гидроксид меди(II) важным компонентом в различных химических процессах и синтезе органических соединений.
Гидроксид меди 2: основные реакции и взаимодействие с другими веществами

Гидроксид меди 2 обладает рядом химических свойств, которые определяют его основные реакции и способность взаимодействовать с другими веществами.
| Реакции гидроксида меди 2 | Уравнение реакции |
|---|---|
| Реакция с кислотами | Cu(OH)2 + 2HCl → CuCl2 + 2H2O |
| Реакция с щелочами | Cu(OH)2 + 2NaOH → Cu(OH)2•2NaOH |
| Реакция с аммиаком | Cu(OH)2 + 2NH3 → Cu(NH3)2(OH)2 |
| Реакция с карбонатами | Cu(OH)2 + CO2 → CuCO3 + H2O |
| Реакция с основаниями | Cu(OH)2 + 2KOH → Cu(OH)2•2KOH |
Гидроксид меди 2 также может выполнять функцию оксида меди 2 при нагревании, выделяя воду и образуя оксид меди 2:
2Cu(OH)2 → CuO + H2O
Гидроксид меди 2 также может быть окислен до гидроксида меди 1 с помощью хлорного газа:
2Cu(OH)2 + 4HCl + Cl2 → 2CuCl2 + 5H2O
Такие реакции гидроксида меди 2 являются важными в химии и позволяют использовать его в различных синтетических и аналитических процессах.
Реакция гидроксида меди II с кислотами

При реакции с минеральными кислотами, например, соляной, серной или азотной, гидроксид меди II образует соответствующие соли меди II и воду:
- С реакцией с соляной кислотой образуется хлорид меди II (CuCl2) и вода (H2O):
- 2Cu(OH)2 + 4HCl = 2CuCl2 + 4H2O
- С реакцией с серной кислотой образуется сульфат меди II (CuSO4) и вода (H2O):
- Cu(OH)2 + H2SO4 = CuSO4 + 2H2O
- С реакцией с азотной кислотой образуется нитрат меди II (Cu(NO3)2) и вода (H2O):
- Cu(OH)2 + 2HNO3 = Cu(NO3)2 + 2H2O
Также гидроксид меди II может реагировать с органическими кислотами, например, уксусной или молочной. При этом образуются соответствующие органические соли меди II и вода:
- С реакцией с уксусной кислотой образуется ацетат меди II (Cu(CH3COO)2) и вода (H2O):
- 2Cu(OH)2 + 2CH3COOH = Cu(CH3COO)2 + 2H2O
- С реакцией с молочной кислотой образуется лактат меди II (Cu(C3H5O3)2) и вода (H2O):
- 2Cu(OH)2 + 2C3H6O3 = Cu(C3H5O3)2 + 2H2O
Реакции гидроксида меди II с кислотами широко используются в химических процессах, в синтезе органических соединений и в производстве различных препаратов и каталитических систем.
Взаимодействие гидроксида меди 2 с солями

При взаимодействии с солями разных катионов, гидроксид меди 2 может образовывать осадки или переходить в растворимые комплексные соединения. Одним из таких осадков является осадок гидроксида меди 2, который образуется при реакции с солями щелочных металлов, например, натрия или калия. Эти осадки имеют характерный голубоватый цвет и используются в различных областях применения, включая косметическую, фармацевтическую и керамическую промышленности.
С другой стороны, гидроксид меди 2 может также образовывать растворимые комплексные соединения с солями некоторых металлов, таких как железо или цинк. Эти соединения имеют важное значение в различных химических процессах, таких как каталитические реакции или электрохимические процессы.
Таким образом, взаимодействие гидроксида меди 2 с солями представляет собой сложный процесс, в результате которого могут образовываться различные соединения с разными свойствами. Изучение этих реакций имеет большое значение для понимания химических свойств гидроксида меди 2 и его возможных применений в различных областях науки и технологии.
Процессы окисления и восстановления гидроксида меди 2
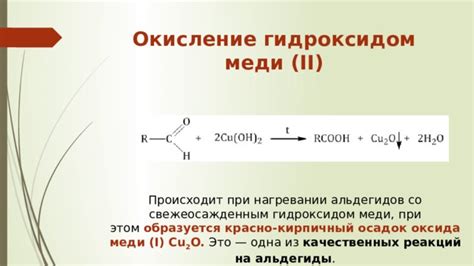
Окисление гидроксида меди 2 происходит при взаимодействии с окислителями. В результате этой реакции гидроксид меди 2 превращается в соединение с более высокой степенью окисления. Например, при взаимодействии гидроксида меди 2 с кислородом происходит образование гидроксида меди 1 (CuOH), который имеет окислительные свойства.
Восстановление гидроксида меди 2 может происходить при взаимодействии с восстановителями. В результате этой реакции гидроксид меди 2 превращается в соединение с более низкой степенью окисления. Например, при взаимодействии гидроксида меди 2 с водородом происходит образование меди (Cu) и воды (H2O).
Процессы окисления и восстановления гидроксида меди 2 могут быть регулированы с помощью катализаторов и изменения условий реакции, таких как температура и среда. Эти процессы широко используются в промышленности для различных химических реакций и синтеза разнообразных соединений.
| Примеры окислителей | Примеры восстановителей |
|---|---|
| Кислород (O2) | Водород (H2) |
| Пероксид водорода (H2O2) | Металлы (Li, Na, K) |
| Хлор (Cl2) | Аммиак (NH3) |
Важно отметить, что окисление и восстановление гидроксида меди 2 являются реверсивными процессами и могут происходить в обе стороны в зависимости от условий реакции и доступности соответствующих реагентов.
Влияние гидроксида меди 2 на органические вещества

Одним из наиболее известных примеров взаимодействия гидроксида меди 2 с органическими веществами является его воздействие на амины. Гидроксид меди 2 может реагировать с аминами и образовывать соответствующие соли. Это свойство может быть использовано в органическом синтезе и аналитической химии.
Другим интересным аспектом влияния гидроксида меди 2 на органические вещества является его роль в окислительно-восстановительных реакциях. Гидроксид меди 2 может служить как окислителем, так и восстановителем при взаимодействии с органическими соединениями. Это может быть использовано для синтеза новых органических соединений или для изменения свойств существующих веществ.
Также следует отметить, что гидроксид меди 2 может взаимодействовать с органическими кислотами, образуя соли. Это свойство может быть использовано для получения новых органических соединений или для исследования их химических свойств.
Наконец, гидроксид меди 2 может проявлять каталитическую активность в реакциях с органическими веществами. Это означает, что он может ускорять реакции, не участвуя в них. Такая активность может быть использована в промышленных процессах или в органическом синтезе для получения желаемых продуктов.
Таким образом, гидроксид меди 2 обладает разносторонним влиянием на органические вещества, что позволяет использовать его в различных областях, включая органический синтез, аналитическую химию и промышленность.